
金秋,是收获的季节。9月以来,重磅药物获批上市的消息不断传出——境内外均未上市的创新药物呋喹替尼胶囊、临床急需罕见病用药依库珠单抗注射液、肝癌治疗新药仑伐替尼等陆续被批准上市。2015年12月~2018年8月,国家药品监管部门对外公布31批优先审评品种名单(一批加快境外已上市创新药在我国上市),将410个品种纳入优先审评通道。今年年初以来,一批临床急需药物上市,涉及肿瘤、艾滋病、丙肝、罕见病以及儿童用药。这些“救命药”的快速上市,得益于药品审评审批制度改革的不断深化和优先审评审批政策的完善和落实。
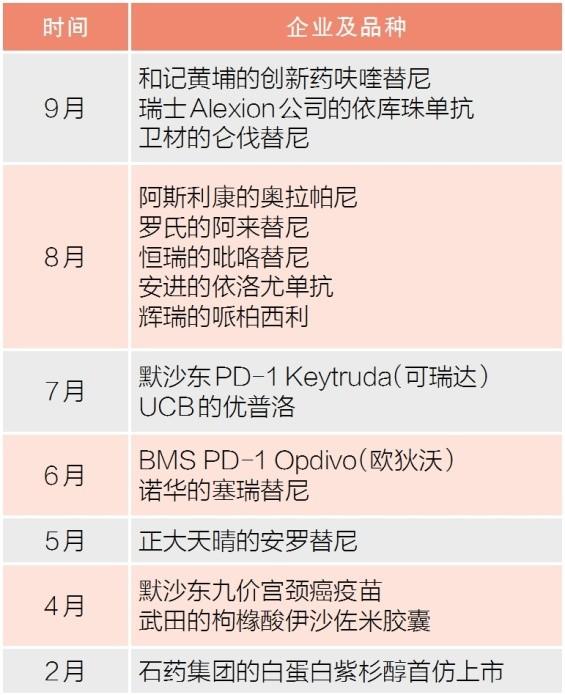
今年通过优先审评审批程序获批上市的部分临床急需药品
以患者为中心
2017年10月,中办、国办印发的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(以下简称《意见》)明确提出,加快临床急需药品、医疗器械审评审批,并强调加快审评审批的药品医疗器械的“临床价值”“急需”等条件。
两个月后,即2017年12月,原国家食品药品监管总局发布《总局关于鼓励药品创新实行优先审评审批的意见》,将18种情形列入优先审评审批范围。此举改变了以往按递交申请时间顺序排队的所谓“公平”原则,更杜绝了通过缴纳“加急费”加快审评的行为。
今年以来,国务院常务会议两次专题研究加快已在境外上市新药进口问题,提出对治疗罕见病药品和防治严重危及生命疾病部分药品简化上市的要求。国家药品监管部门进一步推动简化境外上市新药审批政策措施落地。据评估,纳入加快审批的进口品种通过优先审批通道,进入中国市场的时间可缩短1~2年。仅今年二季度,就有至少七个防治严重危及生命疾病的境外新药获批进入中国市场。
刚刚获得批准进口注册的依库珠单抗注射液由瑞士Alexion公司研发,用于治疗成人和儿童阵发性睡眠性血红蛋白尿症(PNH)和非典型溶血性尿毒症综合征(aHUS),这两种疾病均属于全球罕见疾病。由于依库珠单抗注射液属于临床急需品种,药品审评中心(以下简称“药审中心”)将其纳入优先审评程序进行审评。同时,因其已在国外获批上市,临床疗效明确,风险可控,所以豁免其注册临床试验,并增加其儿童适应证,以使更多患者获益。据了解,依库珠单抗并非唯一一个受益于优先审评制度的治疗罕见病用药。此前,国家药监部门已经通过优先审评批准依达赛珠单抗注射液等罕见病治疗用药上市。另外,多个治疗恶性肿瘤、临床优势明显的临床急需药物也已通过优先审评获批。
“当前药品审评的价值取向是以患者为核心。” 9月6日,药审中心主任许嘉齐在中国药品科学监管大会上明确指出,药品审评要以患者为中心,促进产业转型升级,以临床需求为基础,形成创新驱动环境,以疗效实证证据为标准,满足高质量发展需求。
鼓励创新研发
《意见》明确指出,鼓励新药和创新医疗器械研发,对国家科技重大专项和国家重点研发计划支持,以及由国家临床医学研究中心开展临床试验并经药审、器审中心管理部门认可的新药和创新医疗器械,给予优先审评审批。优先审评审批制度强调“新技术”“新工艺”“国内首仿”等要素,对当下中国医药产业创新发展的引导和推动作用明显。
近日获批的转移性结直肠癌治疗药物呋喹替尼胶囊即为中国医药产业创新的成果。2016年10月,呋喹替尼胶囊成为进入上海市食品药品监管局MAH制度试点品种名单的首个创新药。作为境内外均未上市的创新药,呋喹替尼胶囊于2017年9月获得“优先审评”资格。另外,恒瑞的乳腺癌治疗新药吡咯替尼、正大天晴的肿瘤治疗药安罗替尼、前沿生物的抗艾滋病长效融合酶抑制剂艾博韦泰、石药集团的国内首仿药白蛋白紫杉醇等,均符合优先审评资格,获得快速批准上市。
军事医学科学院附属医院(解放军307医院)乳癌科主任江泽飞认为,国产新药的获批是中国制药企业自主研发实力大幅提升的体现。“可以说,我国优秀的医药企业已逐步实现从仿制药向创新药转型,创新药品质也逐步从Me-Too(化学结构改变小,疗效类似的创新药)走向Me-Better(化学结构改变大,疗效或安全性更有优势的创新药),甚至是Me-Best(化学结构改变大,疗效或安全性显著优于同类产品的创新药)。”江泽飞说。
数据显示,2017年我国创新药注册申请达149个品种,较2016年增长了66%,其中有112个国产品种、37个进口品种。随着包括优先审评审批改革在内的各项药品审评审批制度改革举措落地,国内药品研发创新活力得到进一步释放,扶优汰劣的效果正在显现。
制度建设“永远在路上”
统计数据显示,从《意见》出台至今年6月底,国家药监部门共发布配套文件65个、征求意见稿34个。这些政策在加快新药上市、满足临床急需、鼓励企业创新等方面发挥出积极作用。
科学技术在不断进步,制度和标准也应随之而变。许嘉齐表示,优先审评制度要相应调整,不断更新,不断完善,制度建设“永远在路上”。他对未来优先审评制度的变化作出描述:要从审评时间时限规定的优先,扩展到明确知道审评组织方式的优先;要从相关评价机构分别评估--碎片化评估方式,发展到统一协同审评评价方式;要从原有的对申请资料数据证据的外部审评,发展到对药物研发内部创新的审评;在保证避免利益冲突的前提下,对于创新药审评,审评科学家要融入研发过程,和研发科学家共同工作;全球竞争加速,要从审评后完成标准,发展到边审评边制定标准;要从审评程序规范,发展到审评标准、服务、行为的规范。(记者 刘云涛)

