- 国家市场监督管理总局
- 国家药品监督管理局
- 中国健康传媒集团主办
- 中央新闻网站
简析化妆品飞行检查中的不符合项
梳理国家药品监管局信息发现,2018年7月1日至2019年3月31日,国家药监局共对24家化妆品企业开展了飞行检查,共发现不符合项241个(表1),其中严重缺陷81个、一般缺陷160个。根据飞检结果,国家药监局责令18家企业限期整改,责令6家企业暂停生产。
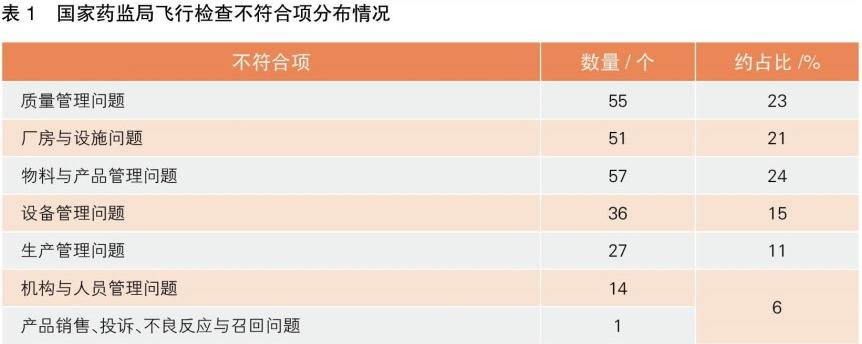
而同期(未统计日常检查数据)广东省药品监管局共对74家化妆品企业开展了飞行检查,只有2家化妆品企业未发现违法违规行为,3家企业在检查时已是停产整改状态,其他共发现589个不符合项(表2)。根据飞检结果,广东省药监局责令33家企业限期整改、36家企业停产整改;存在违法行为的,立案查处。
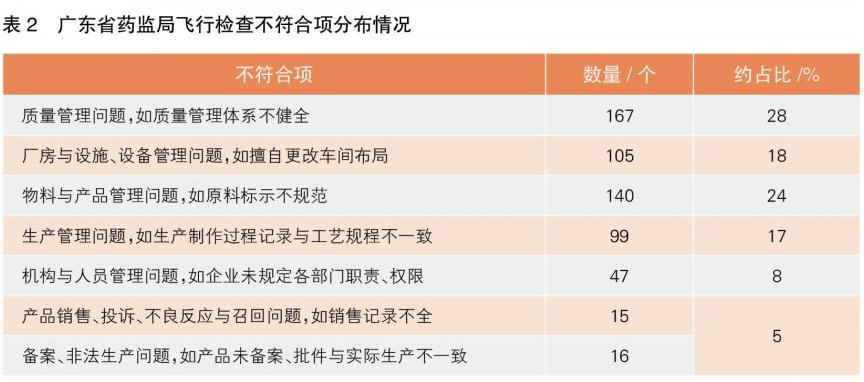
飞行检查结果的公布不仅给问题企业敲了警钟,更有助于引导国内化妆品生产企业提高生产质量管理水平、化妆品经营企业提升经营管理水平,为今后逐步实施化妆品生产、经营质量管理规范打下基础。分析国家药监局和广东省药监局对化妆品企业的飞行检查结果可以发现,不符合项的前三大项为:质量管理问题、物料与产品问题、厂房与设施设备管理问题。
质量管理问题
一是文件记录不规范。部分文件记录存在涂改现象,未按规定对不合格品进行处理;企业未按文件管理制度要求进行文件编写、审核、审批三级控制,未对外来文件进行识别;未建立所用原料的质量检验标准;未按取样规定做好送检样品的标识和储存;企业未落实产品追溯管理制度,未提供物料入库、验收记录,现场抽查的产品无产品留样等。
二是不合格产品乱摆乱放。不合格的物料未清晰标识并专区存放,部分不合格物料未能提供不合格品处理记录;企业未按《不合格品管理制度》规定的规则进行分类、统计;未建立不合格品相关处理记录等。
三是质量管理体系不健全。企业未制定完善的质量管理制度,完善的质量管理制度至少包括:文件管理制度、物料供应管理制度、检验管理制度、放行管理制度等。
四是内部检查制度不完善。企业未制定完善的内审制度,包括内审计划、内审检查表、内审的频率等;还未定期对化妆品生产许可检查要点的实施进行系统、全面的内部检查,确保有效实施等。
五是实验室管理不完善。企业未建立完整的实验室管理制度和检验管理制度;实验室未按检验需要建立相应的功能间,包括微生物检验室、理化检验室;检验过程无详细记录等。
六是企业未严格落实放行制度。部分产品未经检验就出库发货;产品微生物检验未严格按照2015版《化妆品安全技术规范》执行等。
物料与产品问题
一是原料记录与标示不规范。原料入库记录与实际不相符;原料仓储存的原料标识不全,缺少供应商信息、批号、来料日期、有效期等信息;半成品未登记检验日期,无法有效识别储存期限等。
二是原料储存无标识或随意摆放。酒精等危险化学品未按国家有关规定储存;部分原料摆放在仓库外面;半成品静置间中存放半成品的容器未做密封处理;原料储存条件不符合要求,原料仓库有大量杂物等无关物品等。
三是标签不合格。产品标签未标注正确的生产企业信息;标注的许可证号与该企业生产许可证号不一致;未严格按批件载明的配方组织生产等。
四是采购原料时未索要相关资料。未收集供应商相关资料,以确认供应商的资料是否符合要求;未验证供应商提供的样品是否符合产品要求等。
五是留样室的设置与生产规模不相适应;原料仓储区的面积和空间与生产规模不匹配等。
厂房与设施设备问题
一是厂房分区不合理。未严格区分并标识产品状态;未有效管理生产车间人流通道,有交叉污染风险等。
二是企业不能提供有效的车间环境检测报告;现场设施不能达到30万级洁净车间要求。
三是消毒设施等损坏。
四是企业未建立和保存设备采购、安装、确认的文件和记录;部分设备无明确的操作规程。
除上述项目外,企业未备案相关产品或产品备案资料不全、实际生产与备案或注册不一致、非法生产;企业未及时变更质量负责人,质量管理体系未能有效运行;文件记录不一致等,也都是容易出问题的风险点。所以,无论是生产企业,还是监管部门,都要以此为突破口,严守底线,消除隐患,保障消费者的“美丽消费”安全。(作者:上海天祥质量技术服务有限公司 李能)
(责任编辑:)
分享至
右键点击另存二维码!