- 国家市场监督管理总局
- 国家药品监督管理局
- 中国健康传媒集团主办
- 中央新闻网站
每周医药看点(6.25-7.1)
中国食品药品网讯 第五批国家组织药品集中采购中选结果正式公布;《全国深化医药卫生体制改革经验推广基地管理办法(试行)》《抗肿瘤药物临床合理应用管理指标(2021年版)》《2021年国家医保药品目录调整工作方案》《2021年国家医保药品目录调整申报指南》等文件发布;国家药监局公布第四十二批仿制药参比制剂目录……6月25日-7月1日,医药行业的这些事情值得关注。
行业政策动态
1.国务院医改领导小组秘书处印发《全国深化医药卫生体制改革经验推广基地管理办法(试行)》。《办法》共七条,明确了全国医改经验推广基地的评估和退出机制。
2.国家卫生健康委、国家中医药局、中央军委后勤保障部卫生局联合发布《关于进一步加强综合医院中医药工作推动中西医协同发展的意见》,对二级以上综合医院的中医药工作提出了7方面17项系统性要求,同时明确专科医院、传染病医院、妇幼保健机构结合本机构实际情况,参照综合医院完善相关制度,加强中医药工作,促进中西医协同发展。
3.国家发改委、国家卫生健康委、国家中医药管理局、国家疾病预防控制局联合印发《“十四五”优质高效医疗卫生服务体系建设实施方案》。《方案》提出,到2025年,建设 30 个左右国家中医药传承创新中心,重点提升中医药基础研究、优势病种诊疗、高层次人才培养、中医药装备和中药新药研发、科技成果转化等能力,打造“医产学研用”紧密结合的中医药传承创新高地。
4.国家卫生健康委办公厅印发《抗肿瘤药物临床合理应用管理指标(2021年版)》,共涉及限制使用级和普通使用级抗肿瘤药物的使用率等6个指标。
5.国家医保局正式发布《2021年国家医保药品目录调整工作方案》和《2021年国家医保药品目录调整申报指南》,经过三轮调整,新增433个药品进入目录。
6.国家药监局发布《关于进一步明确普通化妆品备案管理工作有关事项的通知》。《通知》指出,普通化妆品备案人提交备案资料即完成备案,产品可上市销售;各省级药监局必须在5个工作日内向社会公开产品备案有关信息;各级监管部门开展监督检查工作中,发现已备案普通化妆品存在备案资料不符合要求、提交虚假备案资料、备案产品存在违法违规情形的,应当按照《化妆品监督管理条例》《化妆品注册备案管理办法》等有关规定,严肃予以查处。
7.国家药监局发布《视力筛查仪注册技术审查指导原则》和《乳腺X射线系统注册技术审查指导原则》2项注册技术审查指导原则,指导相关产品注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
8.国家药监局发布《免于经营备案的第二类医疗器械产品目录》,包括电子血压计、水银血压表、无菌医用脱脂棉、医用脱脂纱布、脱脂棉纱布、避孕套、避孕帽、电动轮椅、手动轮椅、血糖分析仪、自测用血糖监测系统(血糖试纸)、人绒毛膜促性腺激素检测试剂(妊娠诊断试纸)、促黄体生成素检测试剂(排卵检测试纸)13个产品。
9.国家药监局发布《药品监督管理统计报告 (2021 年第一季度)》。《报告》显示,今年1月1日至3月31日,国家药监局批准新药临床试验申请274件,批准中药天然药物及化学药品新上市申请262件;全国共批准各类医疗器械首次注册3358件;批准特殊化妆品首次申报1165件。
10. 国家药监局发布关于实施中国药品监管科学行动计划第二批重点项目的通知,确定并发布了第二批10个重点项目:中药有效性安全性评价及全过程质量控制研究,干细胞和基因治疗产品评价体系及方法研究,真实世界数据支持中药、罕见病治疗药物、创新和临床急需医疗器械评价方法研究,新发突发传染病诊断及治疗产品评价研究,纳米类创新药物、医疗器械安全性有效性和质量控制评价研究,基于远程传输、柔性电子技术及医用机器人的创新医疗器械评价研究,新型生物材料安全性有效性评价研究,化妆品新原料技术指南研究和化妆品安全监测与分析预警方法研究,恶性肿瘤等常见病、多发病诊疗产品评价新工具、新标准和新方法研究,药品、医疗器械警戒技术和方法研究。
11.国家药监局公布第四十二批仿制药参比制剂目录,共包括77个参比制剂,涉及依折麦布辛伐他汀片等药品。
12.国家药监局药审中心(CDE)发布并施行《已上市生物制品药学变更研究技术指导原则(试行)》。该指导原则适用于预防用生物制品、治疗用生物制品和按生物制品管理的体外诊断试剂,从技术角度阐述生物制品上市后注册管理事项变更中药学变更研究的基本思路和关注点。
产品研发/上市信息
1.国家药监局通过优先审评审批程序批准浙江海正药业股份有限公司申报的1类创新药海博麦布片上市。该药品是我国自主研发并拥有自主知识产权的创新药,作为饮食控制以外的辅助治疗,可单独或与HMG-CoA还原酶抑制剂(他汀类)联合用于治疗原发性(杂合子家族性或非家族性)高胆固醇血症。
2.国家药监局通过优先审评审批程序批准江苏艾迪药业股份有限公司申报的1类创新药艾诺韦林片上市。该药用于与核苷类抗逆转录病毒药物联合使用,治疗成人HIV-1感染初治患者。
3.国家药监局批准沛嘉医疗科技(苏州)有限公司生产的创新产品“经导管主动脉瓣系统”注册。该产品由主动脉瓣、配套的输送器及安装使用的压握装载系统组成。用于经心脏团队评估认为需要接受主动脉瓣置换但不适合接受常规外科手术置换瓣膜的重度主动脉瓣钙化性狭窄患者。
4.国家药监局批准山西锦波生物医药股份有限公司“重组Ⅲ型人源化胶原蛋白冻干纤维”上市。该产品用于面部真皮组织填充以纠正额部动力性皱纹(包括眉间纹、额头纹和鱼尾纹),是我国自主研制的首个采用新型生物材料——重组人源化胶原蛋白制备的医疗器械。
5.国家药监局发布4期药品批准证明文件待领信息,共包括98个受理号,涉及辉瑞投资有限公司等企业。(截至7月1日)
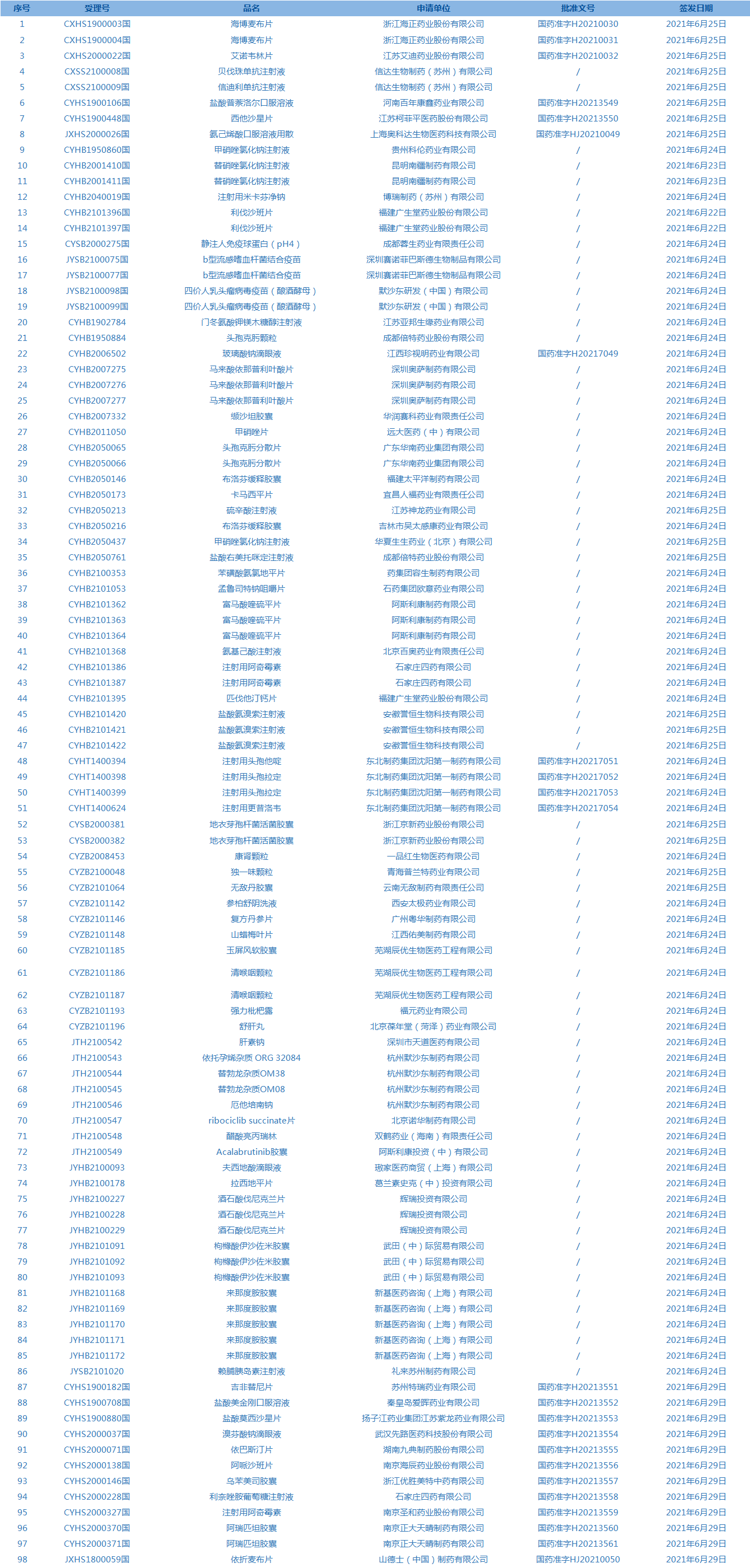
6.国家药监局发布3期医疗器械批准证明文件(准产)待领信息,共包括86个受理号,涉及爱美客技术发展股份有限公司等企业。(截至7月1日)
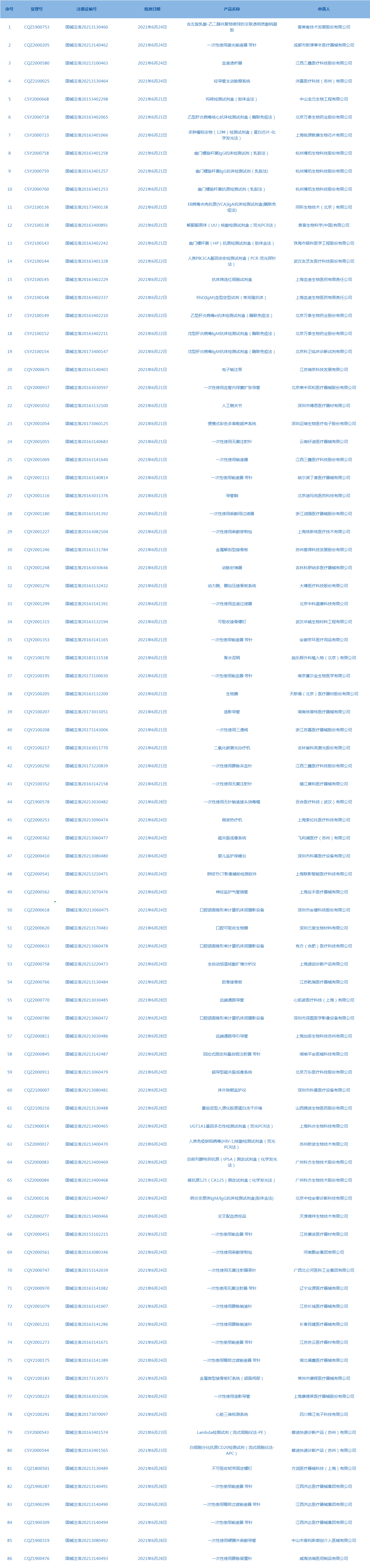
7.CDE网站公示19个仿制药一致性评价任务,涉及头孢呋辛酯分散片等药品。(截至7月1日)
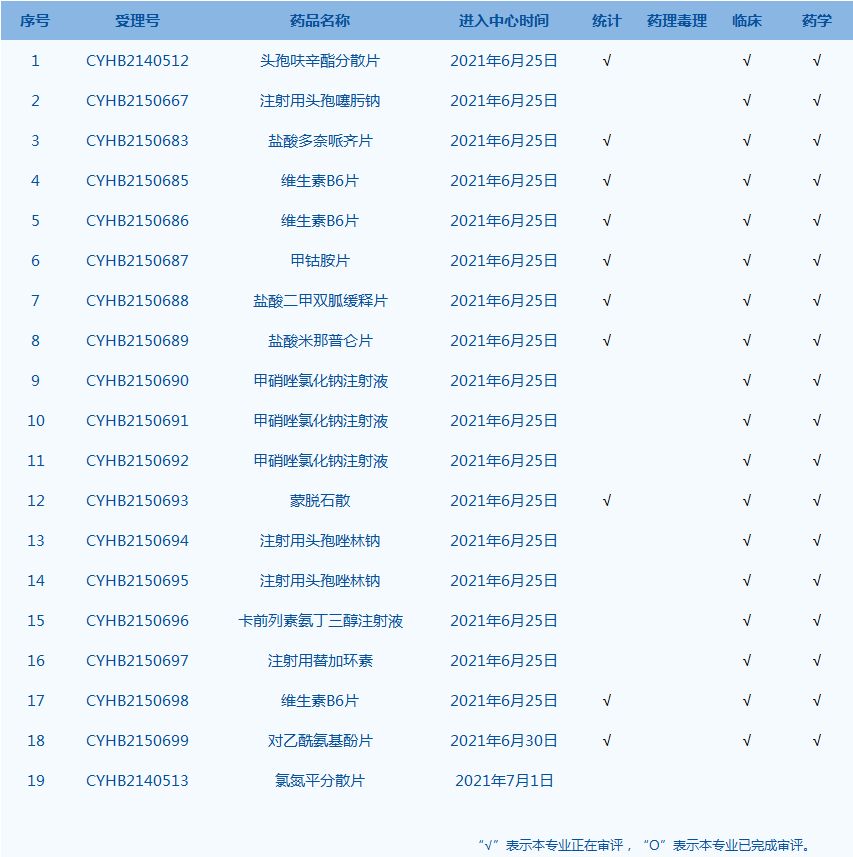
8.CDE承办受理54个新药上市申请,包括HTMC0503片等药品。(截至7月1日)
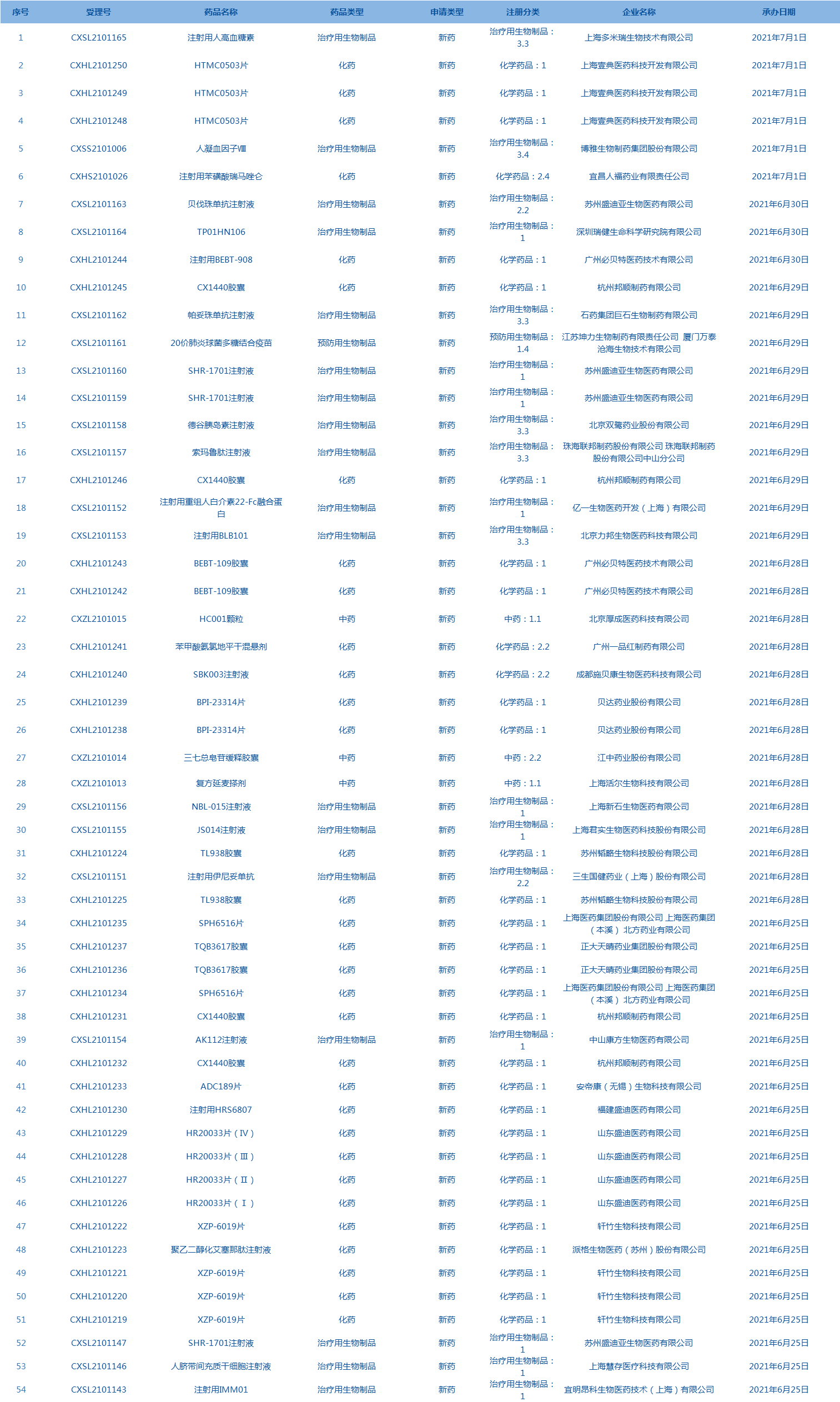
医药企业观察
1.微芯生物发布公告称,日本医药品医疗器械综合机构(PMDA)已批准公司产品西达本胺上市,作为单一疗法治疗复发性或难治性成人T细胞白血病(ATL)。
2.先声药业与Vivoryon Therapeutics共同宣布,双方已建立战略性区域许可合作,在大中华区开发和商业化靶向神经毒性淀粉样蛋白N3pE(pGlu-Aβ)的阿尔茨海默病(AD)治疗药物。根据协议,先声药业将获许在大中华地区开发和商业化两种由Vivoryon公司开发的AD药物,分别是处于临床2b期的靶向N3pE的口服小分子谷氨酰肽环转移酶(QPCT)抑制剂varoglutamstat(PQ912)和处于临床前研究阶段的单克隆N3pE抗体PBD-C06。
3.药明康德子公司合全药业宣布,将在美国特拉华州米德尔顿建设含原料药与制剂的一体化生产基地,进一步拓展平台能力与规模。该基地占地约756,000平方米,预计2024年正式投入运营,将成为合全药业在美国建设的第二个基地,也是该公司在全球范围内布局的第八个研发生产基地。
4.创响生物和安成生物科技宣布,就共同开发安成生物科技研发的新药AC-1101达成协议。根据协议,安成生物科技将授予创响生物AC-1101独家共同开发权,以在一个选定的皮肤病适应症中进行全球1b期临床研究。
5.艾力斯医药宣布,拟与ArriVent Biopharma签署《全球技术转让和授权协议》和《普通股认购协议》,就伏美替尼在海外市场的开发及商业化达成整体合作。
6.贝海生物宣布完成近亿元人民币新一轮融资。本轮融资由国中资本、北京亦尚汇成、嘉兴金琥、珠海科创投等机构共同参与投资。此次募集资金将用于推动其抗肿瘤创新药项目的临床研究,以及支持后续管线的研发和扩大团队规模等。
7.和黄医药于6月30日正式在港交所上市。每股发售价为40.10港元,估计全球发售所得款项净额约为39.50亿港元。
8.百克生物于6月25日正式在上海证券交易所科创板上市。招股书显示,此次该公司在科创板上市,保荐机构为中信证券股份有限公司,发行价为36.35元/股。
药械集中采购
1.上海阳光医药采购网公布第五批国家组织药品集中采购中选结果。本次集采61种药品采购成功,148家企业的251个产品获得中选资格,中选药品平均降价56%,最高降价98.3%。涉及抗感染、消化道、抗肿瘤等多种治疗领域。其中,10家外资企业的11个产品中选,138家国内企业的240个产品中选。外资中选企业数为历次集采最高。
2.内蒙古自治区医保局发布《省际联盟采购办公室关于发布冠脉导引导丝集中带量采购文件(SJLM-14-HC2021-1)的公告》,将组建13省际联盟,开展冠脉导引导丝集中带量采购。本次集采联盟包括内蒙古自治区、山西省、辽宁省、吉林省、黑龙江省、海南省、贵州省、西藏自治区、甘肃省、青海省、宁夏回族自治区、新疆维吾尔自治区、新疆生产建设兵团等省(区、兵团),由内蒙古医保局负责组织以及具体实施。
3.湖北省武汉市药械集中带量采购服务平台发布《武汉市药品集中带量采购品种到期续约或议价办法》。《办法》明确了四类品种的续约/议价办法:国采、国谈、省采、联盟采品种,执行上级集中带量采购结果;因医保变化未完成约定量的,可延长一个采购周期;已完成约定采购量,且品种竞争充分、价格合理,或市场格局未发生变化的,以中选价续约;流标、放弃续约、市场格局发生明显变化的、不能保障供应的纳入竞价,同质量层次不同规格的品种,将调整差比价。
4.黑龙江省药品集中采购网公示了"八省二区"省际联盟药品集中带量采购拟中选结果,14家药企拟中选,美洛西林钠注射剂、克林霉素磷酸酯注射剂、氟尿嘧啶注射剂、利多卡因注射剂、骨化三醇口服常释剂型5个药品流标。
5.吉林省医保局发布《关于做好我省基本医疗保险、工伤保险和生育保险药品目录省增药品2021年消化工作的通知》,明确自2021年8月1日0时起将187个药品调出省增药品目录,报销时间截止到2021年7月31日24时。【中国食品药品网综合整理/刘思慧】
(责任编辑:刘思慧)
分享至
右键点击另存二维码!