- 国家市场监督管理总局
- 国家药品监督管理局
- 中国健康传媒集团主办
- 中央新闻网站
药物警戒 | 药物警戒活动相关报告信息梳理
2019年发布的《药品管理法》明确建立药物警戒制度。为规范药品上市许可持有人和获准开展药物临床试验的药品注册申请人依法承担药物警戒主体责任,2020年12月3日,国家药品监督管理局发布《药物警戒质量管理规范(征求意见稿)》,向社会公开征求意见。
自2018年我国药品监督管理部门加入ICH后,6个E2系列药物警戒指导原则(1.E2A:临床安全性数据管理:快速报告的定义和标准;2.E2B(R3):临床安全数据的管理:快速报告的定义和标准;3.E2C(R2):定期获益-风险评估报告;4.E2D:上市后安全性数据的管理:快速报告的定义和标准;5.E2E:药物警戒计划;6.E2F:研发期间安全性更新报告)也已开始逐步转化实施。药品监管部门通过要求药品注册申请人/持有人及时报告可疑且非预期严重不良反应SUSAR(ICH指导原则E2A、E2B)、定期报告仍处于临床开发中药品的安全性的DSUR(ICH指导原则E2F)、定期报告已批准药品的安全性的PSUR(ICH指导原则E2C(R1)),以及提交定期获益-风险评估报告PBRER(ICH指导原则E2C(R2))对产品的总体利益-风险特征进行评估,在上市申请和/或PSUR中可能提交的ICH指导原则E2E的安全性规范章节,以规划药物警戒活动。
笔者现将药物警戒活动中与临床研究相关的SUSAR和DSUR报告,以及上市后的PSUR和PBRER报告有关要求进行梳理对比,供行业参考。
可疑且非预期严重不良反应报告(SUSAR)
(一)相关法规
2018年1月25日发布的《总局关于适用国际人用药品注册技术协调会二级指导原则的公告》明确,自2018年5月1日起,药物临床研究期间报告严重且非预期的药品不良反应适用《E2A:临床安全数据的管理:快速报告的定义和标准》《M1:监管活动医学词典(MedDRA)》和《E2B(R3):临床安全数据的管理:个例安全报告传输的数据元素》。
为落实上述公告内容,2018年4月27日,CDE发布《药物临床试验期间安全性数据快速报告的标准和程序》,自2018年5月1日后开始实施的临床试验,按照该标准和程序执行。
2018年7月27日,国家药品监督管理局发布《关于调整药物临床试验审评审批程序的公告》,明确:对于药物临床试验期间出现的可疑且非预期严重不良反应和毒理研究提示重大安全性风险信号,申请人应按照《药物临床试验期间安全性数据快速报告标准和程序》中相关要求向药审中心递交(个例)安全性报告。2020年3月30日发布的《药品注册管理办法》中固化该要求,第三章第二十八条明确规定,对于药物临床试验期间出现的可疑且非预期严重不良反应和其他潜在的严重安全性风险信息,申办者应当按照相关要求及时向药品审评中心报告。2020年7月1日,国家药监局药品审评中心发布的《药物临床试验期间安全信息评估与管理规范(试行)》第二章第四条规定,临床试验期间,申请人应通过药物警戒电子传输系统(PV系统)及时提交可疑且非预期严重不良反应(SUSAR)个例报告,通过药审中心网站按时提交其它潜在的严重安全性风险信息报告。SUSAR个例报告、其它潜在的严重安全性风险信息报告相关要求,按照药审中心发布的《药物临床试验期间安全性数据快速报告标准和程序》执行。
(二)报告范围
1.申请人获准开展药物(包括化药、中药及生物制品)临床试验后,对于临床试验期间发生的(包括中国境内和境外)所有与试验药物肯定相关或可疑的非预期且严重的不良反应(SUSAR),以及其他潜在的严重安全性风险信息【注:临床试验包含与新药(中药、化药、生物制品)注册申请有关的Ⅰ、Ⅱ、Ⅲ期临床试验,批件中有特别要求的Ⅳ期临床试验,承诺性临床试验,需要开展临床试验的已上市产品申请增加新的人群或新的适应症,以及需要开展临床试验的已上市产品的重大改变(如新剂型、新给药途径、新生产工艺)等。批件中无特别要求的Ⅳ期临床试验不按此要求报告,可按上市后相关要求进行报告】。
2.以下三种情况,也应该进行快速报告:(1)以上临床试验期间,申请人从其它来源获得的与试验药物相关的非预期严重不良反应及其他潜在严重安全性风险的信息;(2)申请人和研究者在不良事件与药物因果关系判断中不能达成一致时,其中任一方判断不能排除与试验药物相关的情形;(3)临床试验结束或随访结束后至获得审评审批结论前发生的严重不良事件,由研究者报告申请人,若属于非预期严重不良反应,也应进行快速报告。
(三)报告方式
通过药物警戒电子传输系统(PV系统)及时提交。
(四)报告时限
1.快速报告开始时间为临床试验批准日期/国家药品审评机构默示许可开始日期,结束时间为国内最后一例受试者随访结束日期。对于国际多中心临床研究,“临床试验期间”SUSAR快速报告是指从临床试验批准日期/国家药品审评机构默示许可开始日期开始,至全球最后一例受试者随访结束日期。
2.根据严重不良事件的性质(类别)按以下时限向国家药品审评机构快速报告:(1)对于致死或危及生命的非预期严重不良反应,申请人应在首次获知后尽快报告,但不得超过7天,并在随后的8天内报告、完善随访信息(申请人首次获知当天为第0天);(2)对于非致死或危及生命的非预期严重不良反应,申请人应在首次获知后尽快报告,但不得超过15天;(3)申请人在首次报告后,应继续跟踪严重不良反应,以随访报告的形式及时报送有关新信息或对前次报告更改信息等,报告时限为获得新信息起15天内。
研发期间安全性更新报告(DSUR)
(一)相关法规
国家药品监督管理局2018年7月27日发布的《关于调整药物临床试验审评审批程序的公告》第十五条规定,申请人在获得首次临床试验许可后,应定期向药审中心提供药物研发期间安全性更新报告,包括全球研发和上市状况、正在进行中和已完成的临床试验、新增的安全性结果、重大生产变更、整体安全性评估、重要风险总结、获益—风险评估和下一年总体研究计划等内容。一般每年一次,于药物临床试验许可后每满一年后的两个月内提交。药审中心可以根据审查情况,要求申请人调整报告周期。逾期未提交的,申请人应暂停药物临床试验。新《药品注册管理办法》对相关内容进行了固化。
2019年11月12日,国家药品监督管理局发布《关于适用<E1:人群暴露程度:评估非危及生命性疾病长期治疗药物的临床安全性>等15个国际人用药品注册技术协调会指导原则的公告》,明确适用《E2F:研发期间安全性更新报告》及《E2F示例》。
2020年7月1日CDE发布的《药物临床试验期间安全信息评估与管理规范(试行)》第二章第四条规定,临床试验期间,申请人应通过药审中心网站按时提交研发期间安全性更新报告(DSUR)。DSUR相关要求按照药审中心发布的《研发期间安全性更新报告管理规范(试行)》执行。临床试验期间发生临床试验方案变更、非临床或者药学的变化或者有新发现的,申请人应充分评估对受试者安全的影响。评估认为不影响受试者安全的,应在DSUR中报告;如果可能增加受试者安全性风险的,应当提出补充申请。7月1日,CDE同时发布了《研发期间安全性更新报告管理规范(试行)》,规范报告的撰写和管理,并明确:原国家食品药品监督管理局药品审评中心《关于化学药IND申请药学研究数据提交事宜的通知》(2012年5月10日发布)中要求的《化学药IND申请药学研究年度报告(试行)》与研发期间安全性更新报告统一,不再单独提交;申请人应按照ICH E2F《研发期间安全性更新报告》的要求准备、撰写和提交DSUR。
(二)报告范围
1.申请人获准开展药物(包括中药、化学药及生物制品)临床试验后,均应向CDE提交DSUR。
2.DSUR中应包含报告周期内收集到的与药物(无论上市与否)相关的安全性信息全面深入的年度回顾和评估,应讨论报告周期内发现的所有安全性问题,不应作为新的重要安全信息的初始报告途径,也不应作为新的安全问题的检出途径。
3.DSUR侧重研究药物,只有当对照药物与临床试验受试者的安全相关时,才需提供对照药物的信息。
4.DSUR应包含与所有剂型和规格、所有适应症以及研究中接受研究药物的患者人群相关的数据(化学药和生物制品应按照相同活性成分,中药按照相同处方进行准备)。如果相关信息无法获得(如申请人尚未获得数据),申请人应在DSUR的前言部分予以解释说明。
(三)报告方式
通过CDE官网“申请人之窗”“研发期间安全性相关报告递交”栏目递交。
【注:2019年4月26日,CDE官网“申请人之窗”开通“研发期间安全性相关报告递交”栏目,“研发期间安全性更新报告”“非个例的潜在严重安全性风险信息报告”及“其他研发期间安全性相关报告(如:重要已识别风险的报告,采取紧急安全性措施的报告,及申请人判断不需按照补充申请申报的与安全性相关的方案变更等)”,以电子递交形式提交相关报告。《药物临床试验期间安全性数据快速报告标准和程序》中要求的其他非个例的潜在严重安全性风险信息的快速报告不再通过邮件递交。】
(四)报告时限
1.原则上应将药物临床试验在境内或者全球首次获得临床试验许可日期(即“国际研发诞生日”,以下简称DIBD)的月和日,作为年度报告周期的起始日期。首次提交应在境内临床试验获准开展后第一个DIBD后两个月内完成,后续提交也应以DIBD为基准。
2.应持续提交至该药物境内最后一个上市许可申请提交,或者在境内不再继续进行研发时为止。最后一次提交时应附说明文件,说明该次提交为在境内的最后一份DSUR,并说明申请人是否还在其他国家或者地区继续进行临床试验。
定期安全性更新报告(PSUR)
(一)相关法规
为加强药品上市后管理,2011年5月4日原卫生部发布的《药品不良反应报告和监测管理办法》(以下简称81号令)中明确要求生产企业需提交定期安全性更新报告(第三十六至四十条对定期安全性更新报告作出明确规定)。为落实81号令有关要求,规范和指导药品生产企业撰写药品定期安全性更新报告,在主要参考ICH E2C(R1)《上市药品定期安全性更新报告(Periodic Safety Update Reports for Marketed Drugs,PSUR)》内容的基础上,原国家食品药品监督管理局制定了《药品定期安全性更新报告撰写规范》,并于2012年9月6日发布执行。
(二)报告范围
1.取得药品批准证明文件的上市后药品(对于实施批准文号管理的原料药、辅料、体外诊断试剂,对于实施批准文号管理的中药材、中药饮片以及进口中药材,以及对于境内药品生产企业接受境外委托生产但未获得我国批准证明文件的产品,不需要提交PSUR)。
2.对上市后药品的不良反应报告和监测资料进行定期汇总分析,汇总国内外安全性信息,进行风险和效益评估。
3.对于同一活性成分药品有多个批准证明文件【涵盖不同给药途径、适应症(功能主治)或者目标用药人群等】,可以按照一个批准证明文件提交一份PSUR;也可以遵循化学药和生物制品按照相同活性成分、中成药按照相同处方组成报告《定期安全性更新报告》。在一份《定期安全性更新报告》内,可以根据药物的不同给药途径、适应症(功能主治)或目标用药人群进行分层。
(三)报告方式
通过国家药品不良反应监测系统报告《定期安全性更新报告》。
(四)报告时限
1.对于设立新药监测期的国产药品,应当自取得批准证明文件之日起每满1年提交一次定期安全性更新报告,直至首次再注册,之后每5年报告一次;其他国产药品,每5年报告一次。
2.首次进口的药品,自取得进口药品批准证明文件之日起每满1年提交一次定期安全性更新报告,直至首次再注册,之后每5年报告一次。
3.数据汇总时间以取得药品批准证明文件的日期为起点计,上报日期应当在汇总数据截止日期后60日内。可以提交以国际诞生日(IBD,在世界上任何国家或地区的首次上市批准)为起点计的《定期安全性更新报告》,但如果上述报告的数据截止日早于我国要求的截止日期,应当补充这段时期的数据并进行分析。
定期获益-风险评估报告(PBRER)
(一)相关法规
2020年7月21日,国家药品监督管理局发布《关于可适用<E2C(R2):定期获益-风险评估报告(PBRER)>国际人用药品注册技术协调会指导原则的公告》,明确:自公告发布之日(7月21日)起,药品上市许可持有人提交定期安全性更新报告可适用《E2C(R2):定期获益-风险评估报告(PBRER)》国际人用药品注册技术协调会三级指导原则。药品上市许可持有人可以提交PBRER,也可按照81号令和《国家食品药品监督管理局关于印发药品定期安全性更新报告撰写规范的通知》的要求提交报告。
(二)报告范围
1.在国际诞生日或药物开发的国际诞生日(DIBD,在任何国家和地区进行干预性临床试验的首次授权日期)起可能获得的任何相关有效性/疗效信息的背景下,从可用数据来源对相关的新的安全性信息进行评估,是对总体数据的评估。
2.PBRER应包括产品的累积知识,同时将重点放在新信息上。
3.上市后研究的相关信息或未经批准的适应症或人群的临床试验的相关信息也应包括在PBRER中。
(三)报告方式
通过国家药品不良反应监测系统报告(注:药品上市许可持有人可以使用PBRER代替PSUR递交)。
(四)报告时限
1.向监管机构提交PBRER报告和提交报告的频率需要遵守国家或区域监管要求,通常取决于批准日期、产品在市场上的时间长短、对产品的利益-风险特征的了解程度等因素。PBRER格式和内容旨在适用于报告期为6个月或正常的定期报告。一但药物已经上市好几年,国家或区域的法规可能允许提交的频率延长到更长的时间间隔。
2.数据锁定时间:对于新批准的产品,一般区域要求6个月的周期(至少在批准后的前2年);对于常规/定期提交的PBRER,报告应基于累积数据,间隔数据集为6个月或其倍数。
3.数据锁定点与提交之间的时间间隔:覆盖6个月或12个月的期限,70个日历日内;间隔时间超过12个月,90个日历日内。
DSUR、PSUR和PBRER对比
(一)DSUR & PSUR
1.从报告范围看,DSUR侧重于研究药物,PSUR针对已获批上市药物的安全性进行定期报告。
2.从内容上看,DSUR和PSUR很可能会有重叠,并有一定的重复。如:上市后的信息可能会与临床研发相关,因此应在DSUR中报告。DSUR中可能会包含已上市药物在临床试验中获得的安全性结果,属于上市后安全性信息,也应在PSUR中报告。因此,《研发期间安全性更新报告管理规范》第八条规定,当药物在境内外获得了上市许可,如申请人需要,可以在IBD的基础上准备和提交DSUR。调整后的首次提交,报告周期不应超过一年。
3.从接收部门看,DSUR应提交至药品审评中心,PSUR应提交至药品评价中心。
(二)PSUR & PBRER
PSUR主要目的是全面了解经批准的药品的安全性。PBRER的主要目的是对关于药品风险的新的或新出现的信息及其对已批准的适应症的益处进行全面、简明和批判性的分析,以便对产品的总体利益-风险特征进行评估。PBRER比PSUR更为重视利益,特别是当风险评估发生重要变化时;比PSUR更加强调药品的累积知识,并将重点放在新信息上。
(三)PBRER & DSUR
鉴于DSUR是对研究药物DIBD为基准的相关安全性信息进行全面深入的年度回顾和评估;PBRER是对药物IBD或DIBD为基准的可能获得任何相关有效性/疗效信息,从可用数据来源对相关的新的安全性信息进行评估。因此,如果药品的DSUR的DIBD与ICH E2F中建议的同一产品的PBRER的IBD一致,只要数据锁定点是相同的,即当每个报告覆盖基于IBD的一年间隔时,则DSUR多个章节的内容可以在PBRER中使用。
(四)DSUR、PSUR和PBRER资料要求对比
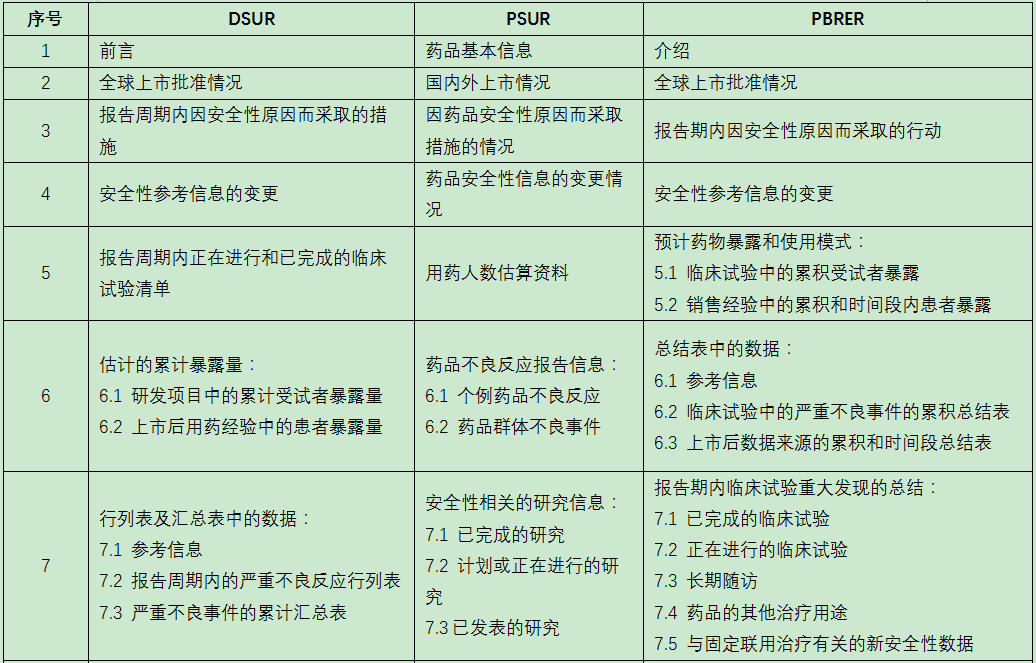
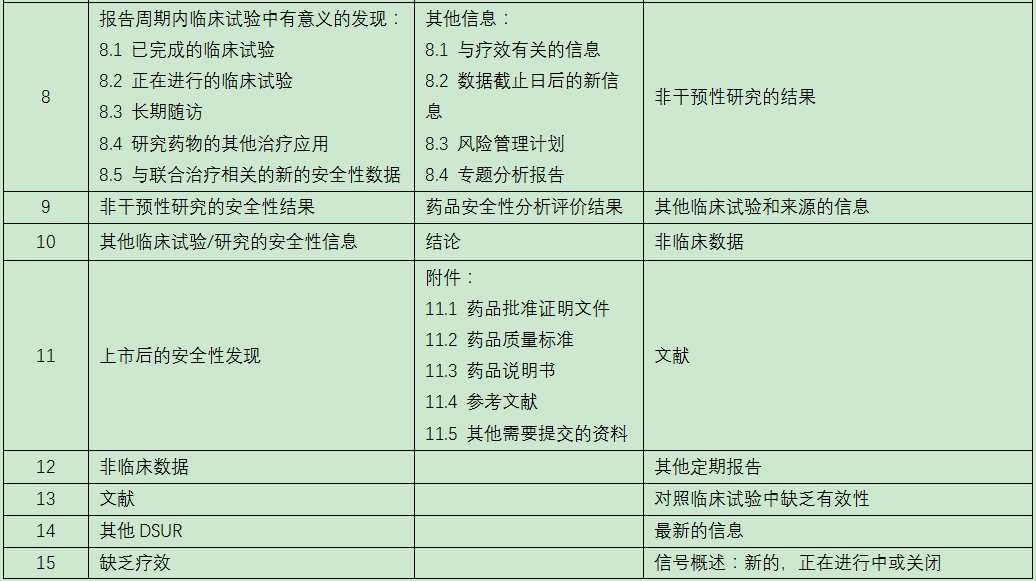
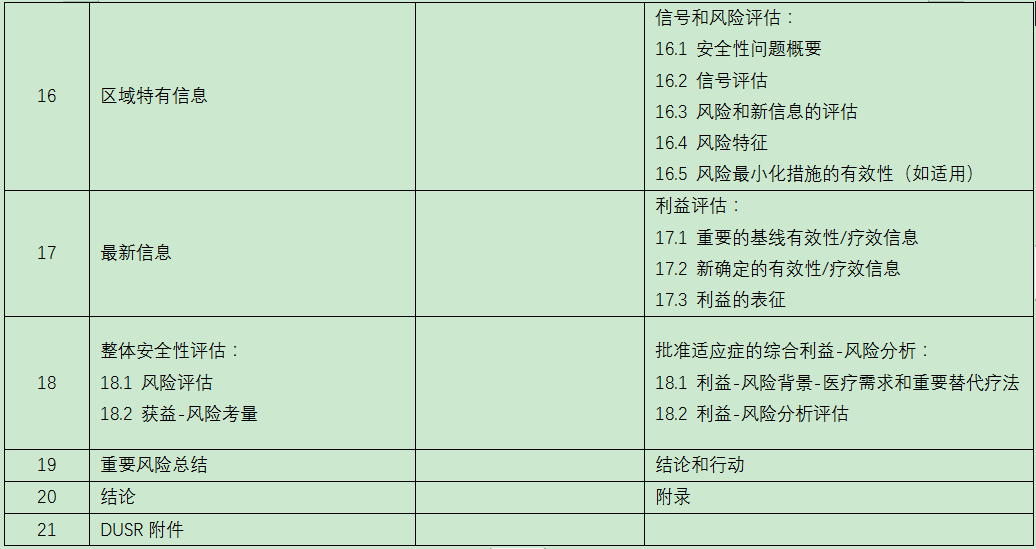
(王海燕)
本文仅代表作者观点,不代表本站立场。
(责任编辑:李硕)
分享至
右键点击另存二维码!