- 国家市场监督管理总局
- 国家药品监督管理局
- 中国健康传媒集团主办
- 中央新闻网站
2020盘点:我国2类改良型新药分析
改良型新药是当前新药研发的热点方向之一。2020年12月31日,国家药监局药品审评中心(CDE)收官发布的20多个指导原则中,即包括《化学药品改良型新药临床试验技术指导原则》,以进一步明确我国改良型新药的临床优势定义,并鼓励临床开发。
以下是2020年我国2类改良型新药的注册申报及批准状态。
改良新药2.1类IND/NDA受理-批准统计
2类改良型新药是指在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势的药品。
细分到2.1类改良型新药,是指含有用拆分或合成等方法制得的已知活性成分的光学异构体,或对已知活性成分成酯,或对已知活性成分成盐(包括含有氢键或配位键的盐),或改变已知盐类活性成分的酸根、碱基或金属元素,或形成其他非共价键衍生物(如络合物、螯合物或包合物),且具有明显临床优势的原料药及其制剂。
2020年,2.1类改良型新药中CDE承办的IND品种仅有4个,其中由江苏恒瑞开发的注射用HR18034分别进行了2.1和2.2类的注册申报。
NDA品种中,仅有南京圣和药业的左奥硝唑片获批生产。
表1.1 2020年国内化药2.1类IND品种受理统计
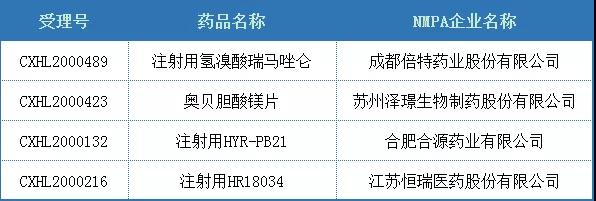
(数据源:药智数据)
改良型新药2.2类IND/NDA受理-批准统计
2.2类改良型新药,是指含有已知活性成分的新剂型(包括新的给药系统)、新处方工艺、新给药途径,且具有明显临床优势的制剂。该类别为国内2类改良型新药的重要开发方向,故每年的注册申报品种数量及获批数量都相对较多。
IND品种方面,有超过40个品种获得了CDE的承办。其中,南京绿叶制药的盐酸伊立替康氟脲苷脂质体注射液是以化药2.2/2.3注册申报,江苏恒瑞的盐酸伊立替康脂质体注射液是以化药2.2/2.4注册申报,江苏奥赛康药业的注射用格列本脲是以化药2.2/2.4注册申报。
表2.1 2020年国内化药2.2类IND品种受理统计
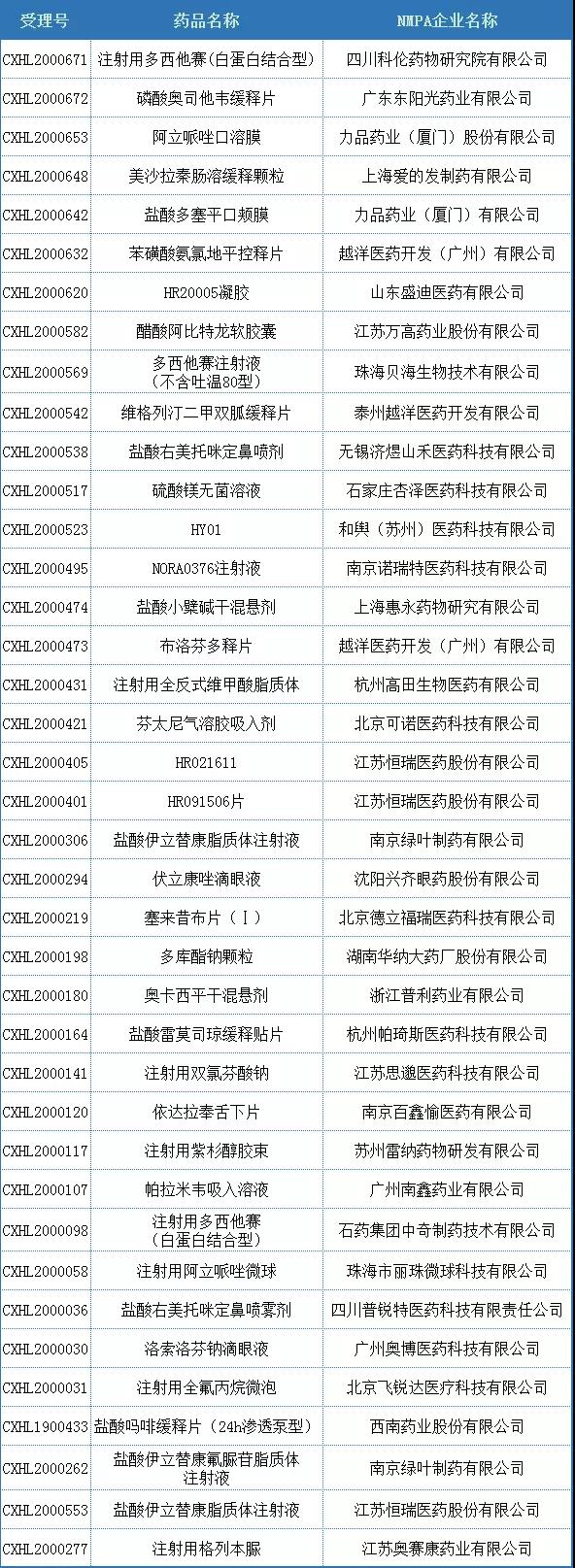
(数据源:药智数据)
NDA品种方面,共有7个品种获CDE承办,其中齐鲁制药申报品种相对较多;而NDA批产品种仅有1个,为江苏豪森的奥氮平口腔速溶膜。
表2.2 2020年国内化药2.2类NDA品种受理统计
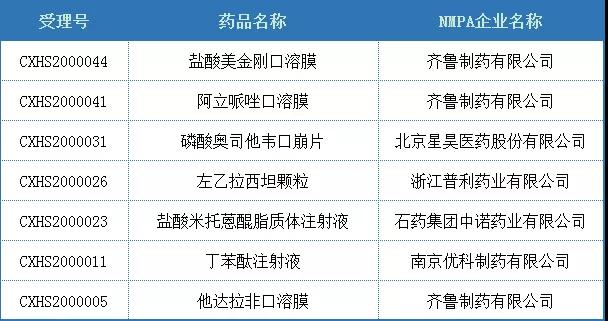
(数据源:药智数据)
改良型新药2.3类IND/NDA受理-批准统计
2.3类改良型新药,是指含有已知活性成分的新复方制剂,且具有明显临床优势。IND品种申报,2020年共6个新复方获得受理。NDA品种申报,仅有1个品种获得受理,为长春海悦药业股份有限公司的XY066胶囊。
表3.1 2020年国内化药2.3类IND品种受理统计
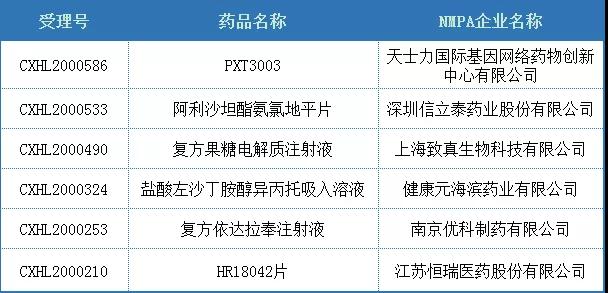
(数据源:药智数据)
改良型新药2.4类IND/NDA受理-批准统计
2.4类改良型新药,为含有已知活性成分的新适应症的制剂,同样为国内对2类改良型新药重要的开发方向之一。
IND品种方面,有近20个化学实体的新适应症获得了CDE的承办。其中,江阴贝瑞森制药有限公司的孟鲁司特钠凝胶是以化药2.4/2.2进行注册申报,江苏恒瑞医药股份有限公司的注射用HR17020是以化药2.4/2.2进行注册申报。
表4.1 2020年国内化药2.4类IND品种受理统计
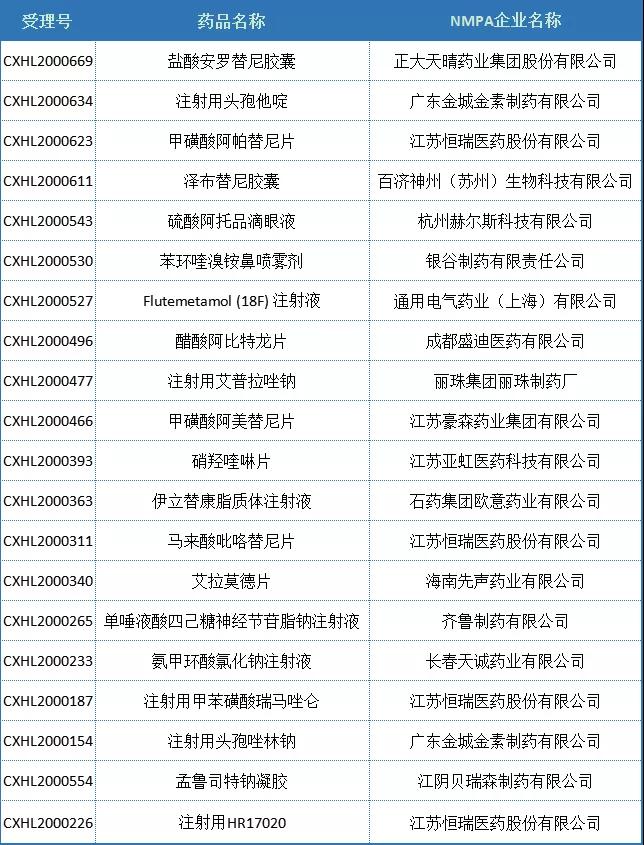
(数据源:药智数据)
NDA品种,2020全年共7个品种获得受理,大多为近年来国内获批上市的1类化药,其中江苏恒瑞有2款产品获得受理,分别为氟唑帕利和阿帕替尼。
表4.2 2020年国内化药2.4类NDA品种受理统计
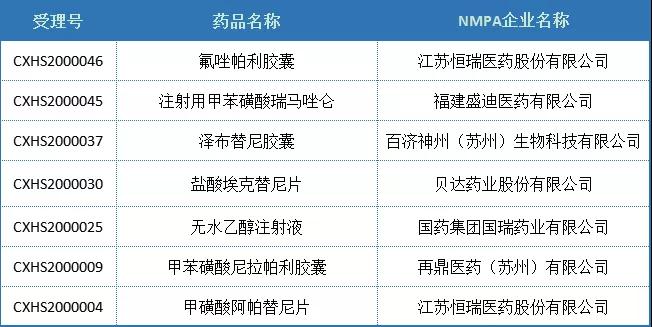
(数据源:药智数据)
此外,NDA品种,2020年共3款品种以化药2.4类获得批准生产,分别为再鼎医药的尼拉帕利、正大天晴的安罗替尼以及阿斯利康的艾司奥美拉唑钠。
表4.3 2020年国内化药2.4类NDA品种批产统计
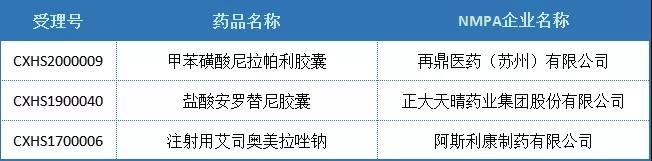
(数据源:药智数据)
综上,从注册分类来看,国内改良型新药的开发整体还是以新制剂和新适应症为主,2.1类和2.3类改良型新药数量相对不多。国产1类新药上市后,伴随着2类改良型新药的注册申报,已从一种趋势变为一种常态,以期获得更大的临床使用范围及适应症市场。且通过多年的统计不难发现,2020年度2类新药的注册申报数量明显增多,国内药企对于2类新药的关注度已明显提升。预计未来,2类新药的注册申报将会成为热点。(中华小吃 药智网)
(责任编辑:刘思慧)
分享至
右键点击另存二维码!